Xantat
Xanthate biasanya merujuk kepada garam asid xantik. Xantat juga boleh merujuk kepada anion [R−O−CS
2]−
atau ester asid xantik. Formula asid xantik ialah R−O−C(=S)−S−H, manakala formula ester asid xantik ialah R−O−C(=S)−S−R', di mana R dan R' ialah kumpulan organil. Garam xantat juga dipanggil O -organyl dithioates. Ester asid xantik juga dipanggil O, S-ester diorganil asid ditiokarbonik. Nama xantat berasal daripada bahasa Yunani Purba ξανθός xanthos, bermaksud "kekuningan, keemasan", dan sememangnya kebanyakan garam xantat berwarna kuning. Mereka ditemui dan dinamakan pada tahun 1823 oleh ahli kimia Denmark William Christopher Zeise. Sebatian organosulfur ini penting dalam dua bidang: penghasilan selofan dan polimer berkaitan daripada selulosa dan (dalam perlombongan) untuk pengekstrakan bijih galas sulfida tertentu. Ia juga merupakan perantara serba boleh dalam sintesis organik.
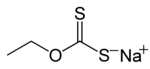

Pembentukan dan struktur sunting
Garam xantat logam alkali dihasilkan melalui rawatan alkohol, alkali, dan karbon disulfida . Proses itu dipanggil xantation. Dalam istilah kimia, alkali bertindak balas dengan alkohol untuk menghasilkan alkoksida, iaitu nukleofil yang menambah atom karbon elektrofilik dalam CS2. Selalunya alkoksida dijana in situ dengan merawat alkohol dengan natrium hidroksida atau kalium hidroksida:
- ROH + CS2 + KOH → ROCS2K + H2O
Sebagai contoh, natrium etoksida memberikan natrium etil xantat . Banyak alkohol boleh digunakan dalam tindak balas ini. Garam xantat gred teknikal biasanya mempunyai ketulenan dengan nilai 90–95%. Kekotoran termasuk logam alkali sulfida, sulfat, tritiokarbonat, tiosulfat, sulfit, atau karbonat serta sisa bahan mentah seperti alkohol dan alkali hidroksida. Garam ini boleh didapati secara komersil dalam bentuk serbuk, butiran, serpihan, batang dan larutan tersedia.
Beberapa garam xantat secara komersial atau berguna termasuk:
- natrium etil xantat CH3CH2OCS2Na
- kalium etil xantat, CH3CH2OCS2K
- kalium isopropil xantat, (CH3)2CHOCS2K[1]
- natrium isobutil xantat, (CH3)2CHCH2OCS2Na
- kalium amil xantat, CH3(CH 2 )4OCS2K
Teras garam xantat -OCS2, seperti karbonat dan ester mempunyai geometri molekul planar trigonal. Atom karbon pusat ialah hibrid sp2.
Tindak balas sunting
Sifat asid-bes sunting
Asid xantatik, dengan formula ROC(S)SH, boleh disediakan dengan merawat xantat logam alkali, cth kalium etil xantat, dengan asid hidroklorik pada suhu rendah. Asid metil dan etil xantik ialah minyak yang larut dalam pelarut organik. Asid Benzil xantik mempunyai bentuk pepejal. Mereka mempunyai pKa berhampiran 2.[2] Sebatian ini secara terma terurai dengan kehadiran asas kepada alkohol dan karbon disulfida.[3]
Asid xantik secara ciri terurai:
- ROCS 2 K + HCl → ROH + CS 2 + KCl
Tindak balas ini adalah kebalikan kaedah untuk penyediaan garam xantat. Perantaraan dalam penguraian ialah asid xantik, ROC(S)SH, yang boleh diasingkan dalam keadaan tertentu.
Reaksi lain sunting
Anion xantat juga mengalami tindak balas alkilasi untuk memberikan ester xantat, yang secara amnya stabil:
- ROCS2K + R′X → ROC(S)SR′ + KX
Ikatan CO dalam sebatian ini terdedah kepada pembelahan oleh deoksigenasi Barton-McCombie, yang membolehkan proses penyahoksigenan alkohol.
Mereka boleh dioksidakan kepada dixantogen disulfida:
- 2 ROCS2Na + I2 → ROC(S)S2C(S)OR + 2 NaI
Asilasi xantat boleh menghasilkan ester alkil xantogen (ROC(S)SC(O)R') dan anhidrida yang berkaitan.
Xantat mengikat kepada kation logam peralihan sebagai ligan bidentat. Kompleks neutral cas ini larut dalam pelarut organik.[4]
Xantat adalah perantara dalam proses penyingkiran Chugaev. Ia boleh digunakan untuk mengawal pempolimeran radikal di bawah proses RAFT, juga dipanggil dengan nama MADIX (reka bentuk makromolekul melalui pertukaran xantat (rekaan makromolekul melalui pertukaran bersaling xantat)).
Aplikasi perindustrian sunting
Selulosa bertindak balas dengan karbon disulfida (CS2) dengan kehadiran natrium hidroksida (NaOH) untuk menghasilkan natrium selulosa xantat, yang apabila peneutralan dengan asid sulfurik (H2SO4) memberikan rayon viscose atau kertas selofan (Sellotape atau Scotch Tape).
Garam xantat (cth. natrium alkil xantat, dixantogen) digunakan secara meluas sebagai agen pengapungan dalam pemprosesan mineral.
Sebatian yang berkaitan sunting
Sebuah sebatian yang jarang ditemui, tioxantat timbul melalui tindak balas CS2 dengan garam tiolat. Contohnya, natrium etiltioxantat mempunyai formula C2H5SCS2Na. Dithiocarbamates juga merupakan sebatian yang berkaitan. Ia timbul daripada tindak balas amina sekunder dengan CS2. Contohnya, natrium dietildithiokarbamat mempunyai formula (C2H5)2NCS2Na.
Kesan alam sekitar sunting
Walaupun boleh terbiodegradasi, kelas bahan kimia ini mungkin boleh memberi ancaman toksik kepada hidupan di dalam air pada kepekatan kurang daripada 1 mg/L.[7] Air di hiliran operasi perlombongan sering tercemar dengan xantat.[8]
Rujukan sunting
- ^ Perumalreddy Chandrasekaran, James P. Donahue (2009). "Synthesis of 4,5-Dimethyl-1,3-Dithiol-2-One". Organic Syntheses. 86: 333. doi:10.15227/orgsyn.086.0333.
- ^ Millican, Robert J.; Sauers, Carol K. (1979). "General acid-catalyzed decomposition of alkyl xanthates". The Journal of Organic Chemistry. 44 (10): 1664–1669. doi:10.1021/jo01324a018.
- ^ Gattow, Gerhard; Behrendt, Werner (1977). Carbon Sulfides and their Inorganic and Complex Chemistry. Stuttgart: Georg Thieme. ISBN 3135262014.
- ^ Haiduc, I. (2004). "1,1-Dithiolato ligands". Comprehensive Coordination Chemistry II. 1. m/s. 349–376.
- ^ Galsbøl, F.; Schäffer, C. E. (1967). Tris (O-Ethyl Dithiocarbonato) Complexes of Tripositive Chromium, Indium, and Cobalt. Inorganic Syntheses. 10. m/s. 42–49. doi:10.1002/9780470132418.ch6. ISBN 9780470132418.
- ^ Siegfried Hauptmann: Organische Chemie, 2. durchgesehene Auflage, VEB Deutscher Verlag für Grundstoffindustrie, Leipzig, 1985, S. 652, ISBN 3-342-00280-8.
- ^ Besser, J.; Brumbaugh, W.; Allert, A.; Poulton, B.; Schmitt, C.; Ingersoll, C. (2009). "Ecological impacts of lead mining on Ozark streams: toxicity of sediment and pore water". Ecotoxicology and Environmental Safety. 72 (2): 516–526. doi:10.1016/j.ecoenv.2008.05.013. PMID 18603298.
- ^ Xu, Y.; Lay, J. P.; Korte, F. (1988). "Fate and effects of xanthates in laboratory freshwater systems". Bulletin of Environmental Contamination and Toxicology. 41 (5): 683–689. doi:10.1007/BF02021019. PMID 3233367.