Asid asetoasetik
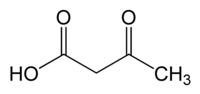
Asid asetoasetik (nama IUPAC: asid 3-oksobutanoik, juga dikenali sebagai asid asetonkarboksilik atau asid diasetik) ialah sebatian organik dengan formula CH3COCH2COOH. Ia merupakan asid beta-keto yang paling ringkat, dan seperti ahli kelas ini yang lain, ia tidak stabil. Bentuk ester metil dan etil yang agak stabil dihasilkan secara besar-besaran secara industri sebagai pendahulu bahan pewarna. Asid asetoasetik ialah asid lemah.[3]
| |
| |
| Nama | |
|---|---|
| Nama IUPAC pilihan
Asid 3-oksobutanoik[1] | |
| Nama IUPAC sistematik
Asid 3-oksobutirik | |
| Nama lain
Asid asetoasetik
Asid diasetik Asid asetilasetik Asid asetonkarboksilik | |
| Pengecam | |
Imej model 3D Jmol
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| KEGG | |
PubChem CID
|
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| C4H6O3 | |
| Jisim molar | 102.09 g·mol−1 |
| Rupa bentuk | Cecair tak berwarna, berminyak |
| Takat lebur | 36.5 °C (97.7 °F; 309.6 K) |
| Takat didih | Terurai |
| Larut | |
| Keterlarutan dalam pelarut organik | Larut dalam etanol, eter |
| Keasidan (pKa) | 3.58[2] |
Kecuali jika dinyatakan sebaliknya, data diberikan untuk bahan-bahan dalam keadaan piawainya (pada 25 °C [77 °F], 100 kPa). | |
| | |
| Rujukan kotak info | |
Biokimia sunting
Di bawah keadaan fisiologi biasa, asid asetoasetik wujud sebagai bes konjugatnya, asetoasetat:
- AcCH
2CO
2H → AcCH
2CO−
2 + H+
Asetoasetat yang tidak terikat dihasilkan terutamanya oleh mitokondrion hati daripada tioesternya dengan koenzim A (KoA):
- AcCH
2C(O)−KoA + OH−
→ AcCH
2CO−
2 + H−KoA
Asetoasetat-KoA itu sendiri terbentuk melalui tiga laluan:
- 3-hidroksi-3-metilglutaril KoA membebaskan asetil KoA dan asetoasetat:
- −
O
2CCH
2−C(Me)(OH)−CH
2C(O)−KoA → −
O
2CCH
2−Ac + Ac−KoA
- −
- Asetoasetil-KoA boleh datang daripada pengoksidaan beta butiril-KoA :
- Et−CH
2C(O)−KoA + 2NAD+
+ H
2O + FAD → Ac−CH
2C(O)−KoA + 2NADH + FADH
2
- Et−CH
- Pemeluwapan pasangan molekul asetil-KoA seperti yang dimangkinkan oleh tiolase.[4]:393
- 2Ac−KoA → AcCH
2C(O)−KoA + H−KoA
- 2Ac−KoA → AcCH
Dalam mamalia, asetoasetat yang dihasilkan dalam hati (bersama dengan dua "badan keton") yang lain dilepaskan ke dalam aliran darah sebagai sumber tenaga semasa tempoh berpuasa, bersenam, atau akibat diabetes melitus jenis 1.[5] Pertama, kumpulan CoA dipindahkan dengan enzim kepadanya daripada suksinil-KoA, menukarkannya kembali kepada asetoasetil-KoA; ini kemudiannya dipecahkan kepada dua molekul asetil-KoA oleh tiolase, dan ini kemudiannya memasuki kitaran asid sitrik. Otot jantung dan korteks buah pinggang lebih cenderung menggunakan asetoasetat berbanding glukosa. Otak menggunakan asetoasetat apabila paras glukosa rendah akibat berpuasa atau diabetes.[4]:394
Sintesis dan sifat sunting
Asid asetoasettik boleh disediakan melalui hidrolisis diketena. Esternya dihasilkan secara analog melalui tindak balas antara diketena dan alkohol,[3] dan asid asetoasetik boleh disediakan melalui hidrolisis spesies ini.[6] Secara amnya, asid asetoasetik dihasilkan pada suhu 0 °C dan digunakan in situ serta-merta.
Ia terurai dalam kadar tindak balas sederhana kepada aseton dan karbon dioksida:
- CH
3C(O)CH
2CO
2H → CH
3C(O)CH
3 + CO
2
Bentuk asid mempunyai separuh hayat 140 minit pada 37 °C dalam air, manakala bentuk asas (anion) mempunyai separuh hayat 130 jam. Iaitu, ia bertindak balas kira-kira 55 kali lebih perlahan.[7] Penyahkarboksilan trifluoroasetoasetat yang sepadan digunakan untuk menyediakan trifluoroaseton:
- CF
3C(O)CH
2CO
2H → CF
3C(O)CH
3 + CO
2
Ia merupakan asid lemah (seperti kebanyakan asid alkil karboksilik), dengan pKa 3.58.
Asid asetoasettik memaparkan pentautomeran keto-enol, dengan bentuk enol distabilkan sebahagiannya melalui konjugasi lanjutan dan ikatan H intramolekul. Keseimbangan sangat bergantung kepada pelarut; dengan bentuk keto mendominasi dalam pelarut berkutub (98% dalam air) dan bentuk enol menyumbang 25-49% bahan dalam pelarut tak berkutub.[8]
Aplikasi sunting
Ester asetoasetik digunakan dalam tindak balas asetoasetilasi yang digunakan secara meluas dalam pengeluaran arilida kuning dan pewarna diarilida.[3] Walaupun ester boleh digunakan dalam tindak balas ini, diketena juga bertindak balas dengan alkohol dan amina kepada derivatif asid asetoasetik yang sepadan dalam proses asetoasetilasi. Contohnya ialah tindak balas dengan 4-amino indana:[9]
Pengesanan sunting
Asid asetoasetik diukur dalam air kencing orang yang menghidap diabetes untuk menguji ketoasidosis[10] dan untuk memantau orang yang menjalani diet ketogenik atau rendah karbohidrat. [11] [12] Ini dilakukan dengan menggunakan batang celupan yang disalut dengan nitroprusida atau reagen yang serupa. Nitroprusida berubah daripada merah jambu kepada ungu dengan kehadiran asetoasetat, bes konjugat asid asetoasetik, dan perubahan warna digredkan oleh mata. Ujian ini tidak mengukur β-hidroksibutirat, keton yang paling banyak dalam badan; semasa rawatan ketoasidosis, β-hidroksibutirat ditukar kepada asetoasetat, menjadikan ujian ini tidak betul selepas rawatan dimulakan,[10] dan mungkin disangka rendah ketika diagnosis.[13]
Ujian serupa digunakan dalam lembu tenusu untuk menguji ketosis.[14]
Rujukan sunting
- ^ "Front Matter". Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book). Cambridge: Royal Society of Chemistry. 2014. m/s. 748. doi:10.1039/9781849733069-FP001. ISBN 978-0-85404-182-4.
- ^ Dawson, R. M. C., et al., Data for Biochemical Research, Oxford, Clarendon Press, 1959.
- ^ a b c Franz Dietrich Klingler; Wolfgang Ebertz (2005). "Oxocarboxylic Acids". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a18_313. ISBN 978-3527306732.
- ^ a b Lubert Stryer (1981). Biochemistry (ed. 2nd).
- ^ Stryer, Lubert (1995). Biochemistry (ed. Fourth). New York: W.H. Freeman and Company. m/s. 510–515, 581–613, 775–778. ISBN 0-7167-2009-4.
- ^ Robert C. Krueger (1952). "Crystalline Acetoacetic Acid". Journal of the American Chemical Society. 74 (21): 5536. doi:10.1021/ja01141a521.
- ^ Hay, R. W.; Bond, M. A. (1967). "Kinetics of decarboxilation of acetoacetic acid". Aust. J. Chem. 20 (9): 1823–8. doi:10.1071/CH9671823.
- ^ Grande, Karen D.; Rosenfeld, Stuart M. (1980). "Tautomeric equilibriums in acetoacetic acid". The Journal of Organic Chemistry. 45 (9): 1626–1628. doi:10.1021/jo01297a017. ISSN 0022-3263.
- ^ Kiran Kumar Solingapuram Sai; Thomas M. Gilbert; Douglas A. Klumpp (2007). "Knorr Cyclizations and Distonic Superelectrophiles". J. Org. Chem. 72 (25): 9761–9764. doi:10.1021/jo7013092. PMID 17999519.
- ^ a b Nyenwe, EA; Kitabchi, AE (April 2016). "The evolution of diabetic ketoacidosis: An update of its etiology, pathogenesis and management". Metabolism: Clinical and Experimental. 65 (4): 507–21. doi:10.1016/j.metabol.2015.12.007. PMID 26975543.
- ^ Hartman, AL; Vining, EP (January 2007). "Clinical aspects of the ketogenic diet". Epilepsia. 48 (1): 31–42. doi:10.1111/j.1528-1167.2007.00914.x. PMID 17241206.
- ^ Sumithran, Priya; Proietto, Joseph (2008). "Ketogenic diets for weight loss: A review of their principles, safety and efficacy". Obesity Research & Clinical Practice. 2 (1): I–II. doi:10.1016/j.orcp.2007.11.003. PMID 24351673.
- ^ Misra, S; Oliver, NS (28 October 2015). "Diabetic ketoacidosis in adults" (PDF). BMJ (Clinical Research Ed.). 351: h5660. doi:10.1136/bmj.h5660. PMID 26510442.
|hdl-access=requires|hdl=(bantuan) - ^ Tatone, EH; Gordon, JL; Hubbs, J; LeBlanc, SJ; DeVries, TJ; Duffield, TF (1 August 2016). "A systematic review and meta-analysis of the diagnostic accuracy of point-of-care tests for the detection of hyperketonemia in dairy cows". Preventive Veterinary Medicine. 130: 18–32. doi:10.1016/j.prevetmed.2016.06.002. PMID 27435643.