Fosfogliserat mutase
Fosfogliserat mutase (PGM) ialah sebarang enzim yang memangkinkan langkah kelapan glikolisis: pemindahan dalaman kumpulan fosfat daripada C-3 kepada C-2 yang mengakibatkan penukaran 3-fosfogliserat (3PG) kepada 2-fosfogliserat (2PG) melalui perantaraan 2,3-bifosfogliserat. Enzim ini dikategorikan kepada dua kelas berbeza, bergantung kepada kofaktor (dPGM) atau bebas kofaktor (iPGM).[1] Enzim dPGM (EC 5.4.2.11) terdiri daripada kira-kira 250 asid amino dan terdapat dalam semua vertebrat serta dalam beberapa invertebrat, kulat dan bakteria. iPGM (EC 5.4.2.12) pula ditemui dalam semua tumbuhan dan alga serta dalam beberapa invertebrat, kulat, dan bakteria positif Gram.[2] Kelas enzim PGM ini berkongsi superkeluarga yang sama dengan fosfatase alkali.[3]
| Keluarga fosfogliserat mutase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Pengenal pasti | |||||||||
| Simbol | PGAM | ||||||||
| Pfam | PF00300 | ||||||||
| InterPro | IPR013078 | ||||||||
| PROSITE | PDOC00158 | ||||||||
| SCOP | 3pgm | ||||||||
| SUPERFAMILY | 3pgm | ||||||||
| |||||||||
| fosfogliserat mutase 1 (otak) | |||||||
|---|---|---|---|---|---|---|---|
 | |||||||
| Pengenal pasti | |||||||
| Simbol | PGAM1 | ||||||
| Simbol alternatif | PGAMA | ||||||
| Gen NCBI | 5223 | ||||||
| HGNC | 8888 | ||||||
| OMIM | 172250 | ||||||
| RefSeq | NM_002629 | ||||||
| UniProt | P18669 | ||||||
| Other data | |||||||
| Nombor EC | 5.4.2.11 | ||||||
| Lokus | Kromosom 10 q25.3 | ||||||
| |||||||
| fosfogliserat mutase 2 (otot) | |||||||
|---|---|---|---|---|---|---|---|
| Pengenal pasti | |||||||
| Simbol | PGAM2 | ||||||
| Gen NCBI | 5224 | ||||||
| HGNC | 8889 | ||||||
| OMIM | 261670 | ||||||
| RefSeq | NM_000290 | ||||||
| UniProt | P15259 | ||||||
| Other data | |||||||
| Nombor EC | 5.4.2.11 | ||||||
| Lokus | Kromosom 7 p13-p12 | ||||||
| |||||||
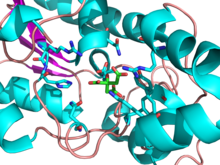
Mekanisme sunting
PGM ialah enzim isomerase yang memindahkan kumpulan fosfat (PO43−) daripada karbon C-3 3-fosfogliserat ke karbon C-2 untuk membentuk 2-fosfogliserat. Terdapat sejumlah tiga tindak balas yang dapat dimangkinkan dPGM: tindak balas mutase menghasilkan penukaran 3PG kepada 2PG dan sebaliknya,[4][5] tindak balas fosfatase menghasilkan fosfogliserat daripada 2,3-bisfosfogliserat,[6][7] dan tindak balas sintase menghasilkan 2,3-bifosfogliserat daripada 1,3-bifosfogliserat, serupa dengan enzim bifosfogliserat mutase. Kajian kinetik dan struktur telah memberi bukti bahawa dPGM dan bisfosfogliserat mutase adalah paralog.[6] Kedua-dua enzim terkandung dalam superkeluarga yang juga mengandungi bahagian fosfatase fosfofruktokinase 2 dan asid prostatik fosfatase.[8]
Tindak balas mutase yang dimangkin melibatkan dua kumpulan fosforil berasingan dan fosfat yang berakhir di karbon 2 bukanlah fosfat yang sama yang dikeluarkan dari karbon 3.Dalam keadaan awal enzim bergantungan kofaktor, tapak aktif mengandungi kompleks fosfohistidina yang dibentuk oleh fosforilasi sisa histidina tertentu.[9] Apabila 3-fosfogliserat memasuki tapak aktif, kompleks fosfohistidina diletakkan untuk memudahkan pemindahan fosfat daripada enzim ke substrat C-2, menghasilkan perantaraan 2,3-bifosfogliserat.
Penyahfosforilan histidina menggerakkan perubahan alosterik setempat dalam konfigurasi enzim yang kini menjajarkan substrat kumpulan fosfat 3-C dengan histidina tapak aktif, dan memudahkan pemindahan fosfat mengembalikan enzim kepada keadaan terfosforilasi awal untuk melepaskan produk 2-fosfogliserat. 2,3-bisfosfogliserat memerlukan kofaktor bagi dPGM. Sebaliknya, kelas iPGM adalah bebas daripada 2,3-bisfosfogliserat, dan memangkinkan pemindahan intramolekul kumpulan fosfat pada monobisfosfogliserat menggunakan perantara fosfoerina.[10]
Ringkasan reaksi sunting
3PG + P-Enzim → 2,3BPG (perantara) + Enzim → 2PG + P-Enzim
Isozim sunting
Mutasi fosfogliserat wujud secara utamanya sebagai dimer dua subunit yang serupa atau berkait rapat dengan jisim kira-kira 32 kDa. Enzim ini terdapat dalam organisma seringkas yis hingga Homo sapiens, dan strukturnya sangat terpelihara dalam kalangan organisma. (Yis PGM adalah ≈74% dipelihara berbanding bentuk mamalia).
Dalam mamalia, subunit enzim kelihatan sama ada dalam bentuk asal otot (jenis m) atau tisu lain (jenis b bagi otak, di mana isozim pada asalnya diasingkan). Sebagai dimer, enzim kemudiannya mempunyai 3 isozim bergantung pada subunit apa yang membentuk keseluruhan molekul (mm, bb atau mb). Jenis mm ditemui terutamanya dalam otot licin hampir secara eksklusif. Isozim mb terdapat dalam otot jantung dan rangka, dan jenis bb terdapat dalam tisu lain.[11] Walaupun ketiga-tiga isozim boleh didapati dalam mana-mana tisu, taburan di atas adalah berdasarkan kelaziman dalam setiap tisu.
Kawal atur sunting
Fosfogliserat mutase mempunyai tenaga bebas Gibbs positif yang kecil, dan tindak balas ini berjalan dengan mudah dalam kedua-dua arah. Oleh kerana ia adalah tindak balas berbalik, ia bukanlah tapak kawal atur utama dalam glikolisis.
Molekul anion seperti vanadat,[12] asetat, ion klorida, fosfat, 2-fosfoglikolat, dan N-[tris(hidroksimetil)metil-2-amino]etanasulfonat dikenali sebagai perencat aktiviti mutase dPGM. Kajian telah menunjukkan dPGM sensitif terhadap perubahan kepekatan ion, di mana peningkatan kepekatan garam mengakibatkan pengaktifan aktiviti fosfatase enzim sambil menghalang aktiviti mutasenya. Garam tertentu seperti KCl diketahui sebagai perencat berpersaingan berkenaan aktiviti 2-fosfogliserat dan mutase.[13] Kedua-dua fosfat dan 2-fosfoglikolat ialah perencat berpersaingan aktiviti mutase berkenaan substrat 2-fosfogliserat dan 2,3-bisfosfogliserat.[14]
Kepentingan klinikal sunting
Pada manusia gen PGAM2 yang mengekod enzim ini terletak pada lengan pendek kromosom 7.
Rujukan sunting
- ^ Johnsen, U; Schönheit, P (September 2007). "Characterization of cofactor-dependent and cofactor-independent phosphoglycerate mutases from Archaea". Extremophiles: Life Under Extreme Conditions. 11 (5): 647–57. doi:10.1007/s00792-007-0094-x. PMID 17576516.
- ^ Jedrzejas, MJ (2000). "Structure, function, and evolution of phosphoglycerate mutases: comparison with fructose-2,6-bisphosphatase, acid phosphatase, and alkaline phosphatase". Progress in Biophysics and Molecular Biology. 73 (2–4): 263–87. doi:10.1016/s0079-6107(00)00007-9. PMID 10958932.
- ^ Galperin, MY; Bairoch, A; Koonin, EV (August 1998). "A superfamily of metalloenzymes unifies phosphopentomutase and cofactor-independent phosphoglycerate mutase with alkaline phosphatases and sulfatases". Protein Science. 7 (8): 1829–35. doi:10.1002/pro.5560070819. PMC 2144072. PMID 10082381.
- ^ Sasaki, R; Utsumi, S; Sugimoto, E; Chiba, H (15 July 1976). "Subunit structure and multifunctional properties of yeast phosphoglyceromutase". European Journal of Biochemistry. 66 (3): 523–33. doi:10.1111/j.1432-1033.1976.tb10578.x. PMID 182494.
- ^ Rose, ZB; Dube, S (25 August 1976). "Rates of phosphorylation and dephosphorylation of phosphoglycerate mutase and bisphosphoglycerate synthase". The Journal of Biological Chemistry. 251 (16): 4817–22. doi:10.1016/S0021-9258(17)33188-5. PMID 8447.
- ^ a b Rose, ZB; Dube, S (10 December 1978). "Phosphoglycerate mutase. Kinetics and effects of salts on the mutase and bisphosphoglycerate phosphatase activities of the enzyme from chicken breast muscle". The Journal of Biological Chemistry. 253 (23): 8583–92. doi:10.1016/S0021-9258(17)34332-6. PMID 213437.
- ^ Sasaki, R; Hirose, M; Sugimoto, E; Chiba, H (10 March 1971). "Studies on a role of the 2,3-diphosphoglycerate phosphatase activity in the yeast phosphoglycerate mutase reaction". Biochimica et Biophysica Acta (BBA) - Enzymology. 227 (3): 595–607. doi:10.1016/0005-2744(71)90010-6. PMID 4328052.
- ^ Wang, Y; Wei, Z; Liu, L; Cheng, Z; Lin, Y; Ji, F; Gong, W (17 June 2005). "Crystal structure of human B-type phosphoglycerate mutase bound with citrate". Biochemical and Biophysical Research Communications. 331 (4): 1207–15. doi:10.1016/j.bbrc.2005.03.243. PMID 15883004.
- ^ Britton, HG; Clarke, JB (March 1969). "The mechanism of the phosphoglycerate mutase reaction". The Biochemical Journal. 112 (1): 10P–11P. doi:10.1042/bj1120010pb. PMC 1187664. PMID 5774486.
- ^ Jedrzejas, MJ; Chander, M; Setlow, P; Krishnasamy, G (28 July 2000). "Mechanism of catalysis of the cofactor-independent phosphoglycerate mutase from Bacillus stearothermophilus. Crystal structure of the complex with 2-phosphoglycerate". The Journal of Biological Chemistry. 275 (30): 23146–53. doi:10.1074/jbc.m002544200. PMID 10764795.
- ^ Omenn, GS; Cheung, SC (May 1974). "Phosphoglycerate mutase isozyme marker for tissue differentiation in man". American Journal of Human Genetics. 26 (3): 393–9. PMC 1762627. PMID 4827367.
- ^ Song, L; Xu, Z; Yu, X (August 2007). "Molecular cloning and characterization of a phosphoglycerate mutase gene from Clonorchis sinensis". Parasitology Research. 101 (3): 709–14. doi:10.1007/s00436-007-0540-9. PMID 17468884.
- ^ Grisolia, S; Tecson, J (11 January 1967). "Mercury-induced reversible increase in 2,3-diphosphoglycerate phosphatase and concomitant decrease in mutase activity of animal phosphoglycerate mutases". Biochimica et Biophysica Acta (BBA) - Enzymology. 132 (1): 56–67. doi:10.1016/0005-2744(67)90191-x. PMID 4291574.
- ^ Grisolia, S; Cleland, WW (March 1968). "Influence of salt, substrate, and cofactor concentrations on the kinetic and mechanistic behavior of phosphoglycerate mutase". Biochemistry. 7 (3): 1115–21. doi:10.1021/bi00843a032. PMID 5690561.
Pautan luar sunting
- Phosphoglycerate+Mutase dalam Tajuk Subjek Perubatan (MeSH) di Perpustakaan Perubatan Negara AS
- PDBe-KB memberikan gambaran semua maklumat struktur dalam PDB berkenaan fosfogliserat mutase 1 manusia