Hidroksil
Kumpulan hidroksil mempunyai formula kimia OH. Ia mengandungi oksigen yang terikat kepada hidrogen. Dalam kimia organik, alkohol dan asid karboksilik mengandungi kumpulan hidroksil. Anion [OH−] iaitu hidroksida terdiri daripada kumpulan hidroksil.
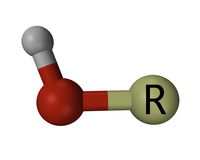
Menurut peraturan IUPAC, istilah "hidroksil" hanya merujuk kepada radikal OH manakala kumpulan berfungsi −OH dipanggil kumpulan hidroksil.[1]
Sifat
suntingAir, alkohol, asid karboksilik, dan sebatian lain yang mengandungi hidroksil boleh dinyahprotonkan dengan mudah. Ciri ini diselaraskan oleh keelektronegatifan oksigen dan hidrogen yang berbeza. Sebatian mengandungi hidroksil ini terlibat dalam ikatan hidrogen yang menyebabkannya pelekatan bersama-sama, membawa kepada takat-takat didih dan lebur yang lebih tinggi daripada sebatian yang kekurangan kumpulan berfungsi ini. Sebatian organik yang sering kurang larut dalam air, menjadi lebih larut dalam air apabila ia mengandungi dua atau lebih kumpulan hidroksil seperti yang ditunjukkan pada gula dan asid amino.
Kejadian
suntingKumpulan hidroksil kerap ditemui dalam kimia dan biokimia. Banyak sebatian organik mengandung kumpulani hidroksil, termasuk asid sulfurik yang paling banyak dihasilkan pada skala industri.
Kumpulan hidroksil mengambil bahagian dalam tindak balas penyahhidratan yang menghubungkan molekul biologi yang mudah kepada rantai panjang. Penghubungan satu asid lemak kepada gliserol untuk membentuk triasilgliserol menyingkirkan −OH dari hujung karboksil kepada hujung asid lemak. Penghubungan dua gula aldehid untuk membentuk disakarida menyingkirkan −OH dari kumpulan karboksil hujung aldehid suatu molekul gula. Penghasilan ikatan peptida untuk menghubungkan dua asid amino untuk menghasilkan protein menyingkirkan −OH dari kumpulan karboksil satu asid amino.
Lihat juga
suntingRujukan
sunting- ^ "Alcohols". IUPAC. Dicapai pada 23 Mac 2015.
Pautan luar
sunting- Reece, Jane; Urry, Lisa; Cain, Michael; Wasserman, Steven; Minorsky, Peter; Jackson, Robert (2011). "Unit 1, Chapters 4 & 5." Dalam Campbell Biologi (Edisi ke-9). Berge, Susan; Emas, Brandy; Triglia, Logan (ed.). San Francisco: Pearson Benjamin Cummings. ISBN 978-0-321-55823-7