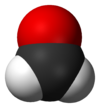
Formaldehid
Formaldehid (atau formalin) ialah sejenis sebatian organik semula jadi dengan formula CH2O (H-CHO). Ia merupakan aldehid (R-CHO) paling mudah, yang juga dikenali dengan nama sistematiknya metanal. Nama biasa bahan ini datangnya dari persamaan ciri dan perkaitannya dengan asid formik.
| |||

| |||
| Nama | |||
|---|---|---|---|
| Nama IUPAC sistematik
Metanal[1] | |||
| Nama lain
Metil aldehid
Metilena glikol Metilena oksida Formalin (larutan akueus) Formol Karbonil hidrida | |||
| Pengecam | |||
Imej model 3D Jmol
|
|||
| 3DMet | |||
| 1209228 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100.000.002 | ||
| Nombor EC |
| ||
| Nombor E | E240 (bahan pengawet) | ||
| 445 | |||
| KEGG | |||
| MeSH | Formaldehyde | ||
PubChem CID
|
|||
| Nombor RTECS |
| ||
| UNII | |||
| Nombor PBB | 2209 | ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| Sifat | |||
| CH2O | |||
| Jisim molar | 30.03 g·mol−1 | ||
| Rupa bentuk | Gas tanpa warna | ||
| Ketumpatan | 0.8153 g/sm³ (−20 °C)[2] | ||
| Takat lebur | −92 °C (−134 °F; 181 K) | ||
| Takat didih | −19 °C (−2 °F; 254 K)[2] | ||
| 400 g dm−3 | |||
| log P | 0.350 | ||
| Tekanan wap | < 1 atm[3] | ||
| Keasidan (pKa) | 13.27 [4][5] | ||
| -18.6·10−6 sm³/mol | |||
| Momen dwikutub | 1.85 D | ||
| Struktur | |||
| C2v | |||
| Bentuk molekul | Satah trigonal | ||
| Farmakologi | |||
| Kod ATC | P53AX19 | ||
| Bahaya | |||
| MSDS | MSDS | ||
| Pengelasan EU | {{{value}}} | ||
| Frasa R | R23/24/25 Templat:R34 Templat:R43 Templat:R45 | ||
| Frasa S | S1/2 S26 S36/37/39 S45 Templat:S51 Templat:S53 Templat:S60 | ||
| NFPA 704 (berlian api) | |||
| Takat kilat | 64 °C (147 °F; 337 K) | ||
| 430 °C (806 °F; 703 K) | |||
| Had letupan | 7–73% | ||
| Dos maut (LD) atau kepekatan dos maut (LC) | |||
LD50 (median dos)
|
100 mg/kg (oral, tikus besar)[8] | ||
LC50 (median kepekatan)
|
333 ppm (tikus kecil, 2 j) 815 ppm (tikus besar, 30 min)[9] | ||
LCLo (paling rendah diketahui)
|
333 ppm (kucing, 2 j)[9] | ||
| NIOSH (Had pendedahan kesihatan AS): | |||
PEL (Dibenarkan)
|
TWA 0.75 ppm ST 2 ppm (dalam bentuk formaldehid dan formalin)[6][7] | ||
REL (Disyorkan)
|
Ca TWA 0.016 ppm C 0.1 ppm [15-minit][6] | ||
IDLH (Bahaya serta-merta)
|
Ca [20 ppm][6] | ||
| Sebatian berkaitan | |||
Aldehid berkaitan
|
Asetaldehid Butiraldehid Dekanal Heptanal Heksanal Nonanal Oktadekanal Oktanal Pentanal Propionaldehid | ||
Sebatian berkaitan
|
metanol asid formik | ||
Kecuali jika dinyatakan sebaliknya, data diberikan untuk bahan-bahan dalam keadaan piawainya (pada 25 °C [77 °F], 100 kPa). | |||
| Rujukan kotak info | |||
Formaldehid bahan pelopor penting kepada banyak bahan dan sebatian kimia yang lain. Pada tahun 1996, kapasiti pengeluaran formaldehid telah dianggarkan sebanyak 8.7 juta tan setiap tahun.[10] Ia digunakan dalam pengeluaran resin tahap industri, contohnya dalam pembuatan papan partikal dan cat lapisan.
Sebatian ini boleh mendatangkan bahaya yang ketara kepada manusia apabila dipertimbangkan penggunaannya yang meluas, serta sifatnya yang toksik dan mudah meruap.[11] Pada tahun 2011, Rancangan Toksikologi Negara Amerika Syarikat menggambarkan formaldehid sebagai "bahan karsinogen manusia yang diketahui".[12][13][14]
Penemuan dan pengeluaran
suntingSejarah
suntingFormaldehid pertama kalinya dilaporkan pada tahun 1859 oleh ahli kimia Rusia bernama Aleksandr Butlerov (1828-86).[15] Penemuan Butlerov ini kemudiannya disahkan oleh August Wilhelm von Hofmann dari Jerman pada 1869.[16][17]
Industri
suntingFormaldehid dihasilkan pada tahap industri melalui pengoksidaan berpemangkin metanol. Pemangkin yang paling biasa digunakan dalam proses ini ialah argentum ataupun campuran ferum dan sebatian oksida molibdenum atau vanadium. Dalam proses formoks, di mana metanol dan oksigen bertindak balas pada suhu sekitar 250-400 °C dalam kehadiran oksida besi dalam kombinasi dengan molibdenum dan/atau vanadium untuk menghasilkan formaldehid menurut persamaan kimia:
- 2 CH3OH + O2 → 2 CH2O + 2 H2O
Pemangkin argentum biasanya berkesan pada suhu yang tinggi iaitu kira-kira 650 °C. Dua tindak balas kimia pada masa yang sama menghasilkan formaldehid: persamaan yang ditunjukkan di atas dan tindak balas pendehidrogenan:
- CH3OH → CH2O + H2
Pada dasarnya, formaldehid boleh dihasilkan oleh pengoksidaan metana, namun ia tidak menguntungkan kerana metanol lebih mudah dioksidakan berbanding metana.
Kegunaan
suntingLarutan akueus formaldehid berguna kerana kebolehannya membunuh kebanyakan bakteria dan fungi (sehingga ke spora-sporanya). Larutan sebegini dipakai secara dalam ubatan untuk mengeringkan kulit, misalnya dalam merawat ketuat.
Apabila formaldehid dirawat dengan fenol, urea atau melamin, ia menghasilkan resin-resin terbitannya yang tersendiri. Polimer ini merupakan bahan pelekat tetap yang biasa digunakan dalam pemasangan papan lapis dan permaidani.
Bahan-bahan berasaskan formaldehid penting dalam industri automobil melalui pembuatan komponen untuk sistem gear, sistem elektrik, blok silinder, panel pintu, gandar-gandar dan kasut brek.
Kilang-kilang tekstil menggunakan resin berasaskan formaldehid sebagai bahan pengemas (finisher) untuk menjadikan fabrik yang terhasil tidak mudah mengedut.[18]
Rujukan
sunting- ^ Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book). Cambridge: The Royal Society of Chemistry. 2014. m/s. 908. doi:10.1039/9781849733069-FP001. ISBN 978-0-85404-182-4.
- ^ a b Formaldehyde (PDF), SIDS Initial Assessment Report, International Programme on Chemical Safety
- ^ Spence, Robert, and William Wild. "114. The vapour-pressure curve of formaldehyde, and some related data." Journal of the Chemical Society (Resumed) (1935): 506-509
- ^ "PubChem Compound Database; CID=712". National Center for Biotechnology Information. Dicapai pada 8 Julai 2017.
- ^ http://chemistry.stackexchange.com/questions/12232/acidity-of-aldehydes
- ^ a b c "NIOSH Pocket Guide to Chemical Hazards #0293". National Institute for Occupational Safety and Health (Institut Keselamatan dan Kesihatan Pekerjaan Negara Amerika Syarikat).
- ^ "NIOSH Pocket Guide to Chemical Hazards #0294".
- ^ http://chem.sis.nlm.nih.gov/chemidplus/rn/50-00-0
- ^ a b "Formaldehyde". Immediately Dangerous to Life and Health. National Institute for Occupational Safety and Health.
- ^ Günther Reuss, Walter Disteldorf, Armin Otto Gamer, Albrecht Hilt "Formaldehyde" in Ullmann's Encyclopedia of Industrial Chemistry, 2002, Wiley-VCH, Weinheim. DOI:10.1002/14356007.a11_619
- ^ "Formaldehyde", Formaldehyde, 2-Butoxyethanol and 1-tert-Butoxypropan-2-ol (PDF), IARC Monographs on the Evaluation of Carcinogenic Risks to Humans 88, Lyon, Perancis: International Agency for Research on Cancer, 2006, m/s. 39–325, ISBN 92-832-1288-6 Templat:11thRoC
- ^ Harris, Gardiner (10 Jun 2011). "Government Says 2 Common Materials Pose Risk of Cancer". New York Times. Dicapai pada 11 Jun 2011.
- ^ National Toxicology Program (Rancangan Toksikologi Negara Amerika Syarikat) (10 Jun 2011). "12th Report on Carcinogens". National Toxicology Program. Dicapai pada 11 Jun 2011.
- ^ National Toxicology Program (10 Jun 2011). "Report On Carcinogens – Twelfth Edition – 2011" (PDF). National Toxicology Program. Dicapai pada 11 Jun 2011.
- ^ A. Butlerow (1859) "Ueber einige Derivate des Jodmethylens" (Dalam sebahagian bahan terbitan metilena iodida), Annalen der Chemie und Pharmacie, vol . 111, muka surat 242–252. Dalam laporan ini, Butlerov menamakan formaldehid yang ditemuinya sebagai "Dioxymethylen" (dioksimetilena atau metilena dioksida) [m.s 247] berdasarkan formula empiriknya (C4H4O4) yang kemudiannya didapati salah.
- ^ In 1867, A. W. Hofmann pertama kalinya mengumumkan kepada Akademi Sains Diraja Prusia mengenai penghasilan formaldehid by dengan mengalirkan wap metanol di udara melalui wayar platinum yang panas. Lihat: A. W. Hofmann (14 Oktober 1867) "Zur Kenntnis des Methylaldehyds" ([Sumbangan] kepada pengetahuan kita terhadap metilaldehid), Monatsbericht der Königlich Preussischen Akademie der Wissenschaften zu Berlin (Laporan Bulanan Akademi Sains Diraja Prusia di Berlin), jld. 8, m.s 665–669. Dicetak semula oleh:
- A.W. Hofmann, (1868) "Zur Kenntnis des Methylaldehyds", Annalen der Chemie und Pharmacie (Catatan Tahunan Kimia dan Farmasi), jld. 145, no. 3, m.s 357–361.
- A.W. Hofmann (1868) "Zur Kenntnis des Methylaldehyds", Journal für praktische Chemie (Makalah Kimia Amali), jld. 103, no. 1, m.s 246–250.
- Hofmann, A.W. (1869). "Beiträge zur Kenntnis des Methylaldehyds". Journal für Praktische Chemie. 107 (1): 414–424. doi:10.1002/prac.18691070161.
- A.W. Hofmann (1869) "Beiträge zur Kenntnis des Methylaldehyds," Berichte der Deutschen Chemischen Gesellschaft (Laporan Persatuan Kimia Jerman), jld. 2, m.s 152–159.
- ^ Read, J. (1935). Text-Book of Organic Chemistry. London: G Bell & Sons.
- ^ "Formaldehyde in Clothing and Textiles FactSheet". Australian National Industrial Chemicals Notification and Assessment Scheme (Skim Penilaian dan Pemakluman Kimia Industri Negara Australia, NICNAS). Mei 2013. Diarkibkan daripada yang asal pada 2014-11-13. Dicapai pada 12 November 2014. Italic or bold markup not allowed in:
|website=(bantuan)