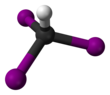
Iodoform
Iodoform (juga dikenali sebagai triiodomethane ) ialah sebatian organoiodin dengan formula kimia CHI
3. Rupa fizikal iodoform ialah krostal bewarna kuning pucat, kristal, dengan bau yang menusuk dan tersendiri (dalam teks kimia lama, bau kadangkala dirujuk sebagai hospital, di mana sebatian itu masih biasa digunakan) dan, sama dengan kloroform, rasa manis. . Ia kadangkala digunakan sebagai pembasmi kuman .

| |||
| |||

| |||
| Names | |||
|---|---|---|---|
| Nama berdasarkan IUPAC
Triiodomethane | |||
Nama lain
| |||
| Identiti | |||
3D model (JSmol)
|
|||
| 1697010 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.000.795 | ||
| EC Number |
| ||
| KEGG | |||
| MeSH | iodoform | ||
PubChem <abbr title="<nowiki>Compound ID</nowiki>">CID
|
|||
| RTECS number |
| ||
| UNII | |||
CompTox Dashboard (<abbr title="<nowiki>U.S. Environmental Protection Agency</nowiki>">EPA)
|
|||
| |||
| |||
| Properties | |||
| CHI3 | |||
| Jisim molar | 393.732 g·mol−1 | ||
| Rupa fizikal | Pale, light yellow, opaque crystals | ||
| Bau | Saffron-like | ||
| Ketumpatan | 4.008 g/cm3[1] | ||
| Takat lebur | 119 °C (246 °F; 392 K)[1] | ||
| Takat didih | 218 °C (424 °F; 491 K)[1] | ||
| 100 mg/L[1] | |||
| Keterlarutan dalam dietil eter | 136 g/L | ||
| Keterlarutan dalam aseton | 120 g/L | ||
| Keterlarutan dalam etanol | 78 g/L | ||
| log <i>P</i> | 3.118 | ||
Henry's law<br><br>constant (kH)
|
3.4 μmol·Pa−1·kg−1 | ||
| −117.1·10−6 cm3/mol | |||
| Structure | |||
| Hexagonal | |||
Coordination geometry
|
Tetragonal | ||
Molecular shape
|
Tetrahedral at C | ||
| Thermochemistry | |||
Muatan haba (C)
|
157.5 J/(K·mol) | ||
Std enthalpy of<br><br>formation (ΔfH⦵298)
|
180.1 – 182.1 kJ/mol | ||
Std enthalpy of
combustion (ΔcH⦵298) |
−716.9 – −718.1 kJ/mol | ||
| Pharmacology | |||
| D09AA13 (WHO) | |||
| Hazards | |||
| GHS labelling: | |||

| |||
| Warning | |||
Hazard statements
|
H315, H319, H335 | ||
Precautionary statements
|
P261, P280, P305+P351+P338 | ||
| NFPA 704 (fire diamond) | |||
| Flash point | 204 °C (399 °F; 477 K) | ||
| Lethal dose or concentration (LD, LC): | |||
LD50 (median dose)
|
|||
| NIOSH (US health exposure limits): | |||
PEL (Permissible)
|
none[3] | ||
REL (Recommended)
|
0.6 ppm (10 mg/m3)[3] | ||
IDLH (Immediate danger)
|
N.D.[3] | ||
| Related compounds | |||
Related compounds
|
| ||
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
Infobox references
| |||

Iodoform selalu disalah panggil sebagai karbon triiodida, [4] salah kerana "karbon triiodide" boleh bermakna CI
3 atau C[I
3], mengabaikan atom hidrogen dalam molekul iodoform, yang membayangkan karbon trivalen atau monovalen dalam iodoform, yang tidak betul. Daripada nama yang salah itu, nama yang betul bagi iodoform atau triiodomethane harus digunakan.
Struktur sunting
Molekul ini menggunakan geometri molekul tetrahedral dengan simetri C3v.
Sintesis dan tindak balas sunting
Sintesis iodoform pertama kali diterangkan oleh Georges-Simon Serullas pada tahun 1822, melalui tindak balas wap iodin dengan wap di atas arang merah panas, dan juga dengan tindak balas kalium dengan iodin etanol dengan kehadiran air; [5] dan pada masa yang sama secara bebas oleh John Thomas Cooper . Ia disintesis dalam tindak balas haloform melalui tindak balas iodin dan natrium hidroksida dengan mana-mana satu daripada empat jenis sebatian organik ini: metil keton (CH
3COR), asetaldehid ( CH
3CHO), etanol (CH
3CH
2OH), dan alkohol sekunder tertentu (CH
3CHROH, di mana R ialah kumpulan alkil atau aril).
Tindak balas iodin dan bes dengan metil keton adalah sangat dipercayai sehingga ujian iodoform (penghasilan mendakan bewarna kuning) digunakan untuk menyiasat kehadiran metil keton. Ini juga berlaku apabila menguji alkohol sekunder tertentu yang mengandungi sekurang-kurangnya satu kumpulan metil dalam kedudukan alfa.
Sesetengah bahan uji (seperti hidrogen iodida ) menukarkan iodoform kepada bentuk diiodometana. Penukaran kepada karbon dioksida juga mungkin: Iodoform bertindak balas dengan perak nitrat berair untuk menghasilkan karbon monoksida . Apabila dirawat dengan serbuk perak unsur iodoform berkurangan, menghasilkan asetilena. Apabila dipanaskan iodoform terurai untuk menghasilkan iodin diatomik, gas hidrogen iodida, dan karbon.
Penghasilan secara semula jadi sunting
Cendawan bonet malaikat mengandungi iodoform, dan mempunyai bau yangmemaparkan ciri iodoform.
Penggunaan sunting
Kompaun ini digunakan secara skala kecil sebagai pembasmi kuman. [2] [6] Sekitar awal abad ke-20, ia digunakan dalam perubatan sebagai pembalut penyembuhan dan antiseptik untuk luka dan kudis dan, walaupun penggunaan ini kini sebahagian besarnya digantikan oleh antiseptik unggul, ia masih digunakan dalam otolaringologi dalam bentuk pes parafin iodoform bismut subnitrat (BIPP) sebagai pembungkus antiseptik untuk bahagian rongga. Ia adalah bahan aktif dalam banyak serbuk telinga untuk anjing dan kucing, bersama-sama dengan zink oksida dan asid propionik, yang digunakan untuk mencegah jangkitan dan memudahkan penyingkiran bulu telinga.
Lihat juga sunting
- Tindak balas iodoform
- Fluoroform
- Kloroform
- Bromoform
Rujukan sunting
Randhawa GK, Graham R, Matharu KS, Bismuth Iodoform Paraffin Paste: Sejarah dan kegunaan. Jurnal British Pembedahan Mulut dan Maksilofasial. 2019;67:E53-E54.
- ^ a b c d e f Ralat petik: Tag
<ref>tidak sah; teks bagi rujukanGESTIStidak disediakan - ^ a b Merck Index, 12 Edition, 5054
- ^ a b c NIOSH Pocket Guide to Chemical Hazards. "#0343".
- ^ "Iodoform".
- ^ Surellas, Georges-Simon (1822), Notes sur l'Hydriodate de potasse et l'Acide hydriodique. -- Hydriodure de carbone; moyen d'obtenir, à l'instant, ce composé triple (dalam bahasa French), Metz, France: Antoine, m/s. 17–20, 28–29 Unknown parameter
|trans_title=ignored (bantuan)CS1 maint: unrecognized language (link) - ^ Lyday, Phyllis A. (2005), "Iodine and Iodine Compounds", Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, m/s. 1–13, doi:10.1002/14356007.a14_381.pub2, ISBN 9783527306732
Pautan luar sunting
- NIOSH Pocket Guide to Chemical Hazards. "#0343" (dalam bahasa Inggeris). National Institute for Occupational Safety and Health (NIOSH).
- MSDS at JT Baker
- A Method for the Specific Conversion of Iodoform to Carbon Dioxide
- Preparation