Asetil-KoA
Asetil-KoA (asetil koenzim A) ialah molekul yang mengambil bahagian dalam banyak tindak balas biokimia dalam metabolisme protein, karbohidrat dan lipid.[2] Fungsi utamanya adalah untuk menghantar kumpulan asetil ke dalam kitaran asid sitrik (kitaran Krebs) untuk dioksidakan bagi penghasilan tenaga.
| |
| |
| Nama | |
|---|---|
| Nama IUPAC pilihan
O1-{(3R)-4-[(3-{[2-(Asetilsulfanil)atil]amino}-3-oksopropil)amino]-3-hidroksi-2,2-dimetil-4-oksibutil} O3-{[(2R,3S,4R,5R)-5-(6-amino-9H-purin-9-il)-4-hidroksi-3-(fosfonooksi)oksolan-2-il]metil} dihidrogen difosfat | |
| Pengecam | |
| |
Imej model 3D Jmol
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.000.719 |
| KEGG | |
| MeSH | Acetyl+Coenzyme+A |
PubChem CID
|
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| C23H38N7O17P3S | |
| Jisim molar | 809.57 g·mol−1 |
| UV-vis (λmax) | 260 nm; 232 nm[1] |
| Keserapan | ε260 = 16.4 mM−1 cm−1 (adenosina)[1] ε232 = 8.7 mM−1 cm−1 (tioester)[1] Δε232 dalam hidrolisis tioester = −4.5 mM−1 cm−1[1] |
Kecuali jika dinyatakan sebaliknya, data diberikan untuk bahan-bahan dalam keadaan piawainya (pada 25 °C [77 °F], 100 kPa). | |
| | |
| Rujukan kotak info | |
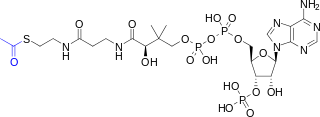
Koenzim A (CoASH atau CoA) terdiri daripada kumpulan β-merkaptoetilamina yang dikaitkan dengan asid pantotenik (vitamin B5) melalui kaitan amida[3] dan ADP dengan 3'-fosforil. Kumpulan asetil (ditunjukkan dengan warna biru dalam rajah struktur di sebelah kanan) asetil-KoA diikat dengan bahagian sulfhidril kumpulan β-merkaptoetilamina. Hubungan tioester ini ialah ikatan "tenaga tinggi" yang begitu reaktif. Hidrolisis ikatan tioester adalah eksergonik (−31.5 kJ/mol).
KoA diasetilkan kepada asetil-KoA oleh pemecahan karbohidrat melalui glikolisis dan oleh pemecahan asid lemak melalui β-pengoksidaan. Asetil-KoA kemudiannya memasuki kitaran asid sitrik, di mana kumpulan asetil dioksidakan kepada karbon dioksida dan air, dan tenaga yang dibebaskan ditangkap dalam bentuk 11 ATP dan satu GTP setiap kumpulan asetil.
Konrad Bloch dan Feodor Lynen telah dianugerahkan Hadiah Nobel dalam Fisiologi atau Perubatan 1964 untuk penemuan mereka yang menghubungkan asetil-KoA dan metabolisme asid lemak. Fritz Lipmann memenangi Hadiah Nobel pada tahun 1953 sempena penemuannya tentang koenzim kofaktor A.[4]
Peranan
suntingAsetil-KoA ialah perantaraan metabolisme yang terlibat dalam banyak laluan metabolik dalam organisma. Ia dihasilkan semasa pemecahan glukosa, asid lemak, dan asid amino, dan digunakan dalam sintesis banyak biomolekul lain, termasuk kolesterol, asid lemak dan badan keton. Asetil-KoA juga merupakan molekul utama dalam kitaran asid sitrik, iaitu satu siri tindak balas kimia yang berlaku dalam mitokondria sel dan bertanggungjawab untuk menjana tenaga dalam bentuk ATP.[5][6]
Di samping itu, asetil-KoA ialah prekursor untuk biosintesis pelbagai bahan kimia asetil, dan bertindak sebagai perantara untuk memindahkan kumpulan asetil semasa biosintesis molekul berasetil tersebut. Asetil-KoA juga terlibat dalam kawal atur pelbagai mekanisme sel dengan menyediakan kumpulan asetil untuk menyasarkan sisa asid amino dalam tindak balas pengasetilan selepas translasi protein.[7]
Biosintesis
suntingPengasetilan KoA ditentukan oleh sumber karbon.[8][9]
Luar mitokondrion
sunting- Dalam tahap glukosa yang tinggi, glikolisis berlaku dengan cepat, sekali gus meningkatkan jumlah sitrat yang dihasilkan daripada kitaran asid sitrik. Sitrat ini kemudiannya dieksport ke organel lain di luar mitokondria untuk dipecahkan kepada asetil-KoA dan oksaloasetat oleh enzim ATP sitrat liase (ACL). Tindak balas utama ini digabungkan dengan hidrolisis ATP.[10][11]
- Dalm tahap glukosa rendah:
- KoA diasetilkan dengan asetat oleh asetil-KoA sintetase (ACS), juga ditambah dengan hidrolisis ATP.[12]
- Etanol juga berfungsi sebagai sumber karbon dalam pengasetilan KoA menggunakan enzim alkohol dehidrogenase.[13]
- Penguraian asid amino ketogenik rantai bercabang seperti valina, leusina dan isoleusina. Asid amino ini ditukar kepada asid α-keto melalui transaminasi, dan akhirnya kepada isovaleril-KoA melalui dekarboksilasi oksidatif oleh kompleks dehidrogenase asid α-keto. Isovaleril-KoA mengalami penyahhidrogenan, karboksilasi dan penghidratan untuk membentuk satu lagi perantara terbitan CoA sebelum ia dibelah menjadi asetil-KoA dan asetoasetat.[14][halaman diperlukan]
Dalam mitokondrion
sunting- Pada tahap glukosa yang tinggi, asetil-KoA dihasilkan melalui glikolisis.[15] Piruvat mengalami dekarboksilasi oksidatif, di mana ia kehilangan kumpulan karboksilnya (sebagai karbon dioksida) untuk membentuk asetil-KoA, mengeluarkan 33.5 kJ/mol tenaga. Penukaran oksidatif piruvat kepada asetil-KoA dirujuk sebagai tindak balas piruvat dehidrogenase, dan dimangkinkan oleh kompleks piruvat dehidrogenase. Penukaran lain antara piruvat dan asetil-KoA adalah mungkin. Sebagai contoh, piruvat format liase menyahkadarkan piruvat kepada asetil-KoA dan asid formik.
- Pada tahap glukosa yang rendah, penghasilan asetil-KoA dikaitkan dengan β-pengoksidaan asid lemak. Asid lemak mula-mula ditukar kepada asil-KoA. Asil-KoA kemudiannya terdegradasi dalam kitaran empat langkah pengoksidaan, penghidratan, pengoksidaan dan tiolisis yang dimangkin oleh empat enzim masing-masing, iaitu asil-KoA dehidrogenase, enoil-KoA hidratase, 3-hidroksiasil-KoA dehidrogenase dan tiolase. Kitaran ini menghasilkan rantai asid lemak baharu dengan dua karbon yang lebih sedikit, dan asetil-KoA sebagai hasil sampingan.[16]
Fungsi
sunting- Kitaran Krebs:
- Dalam satu siri tindak balas kimia, tenaga tersimpan dilepaskan melalui pengoksidaan asetil-KoA yang terbit daripada karbohidrat, lemak dan protein menjadi adenosina trifosfat (ATP) dan karbon dioksida.
- Metabolisme asid lemak
- Asetil-KoA dihasilkan daripada penguraian karbohidrat (glikolisis) dan lipid (β-pengoksidaan). Ia kemudiannya memasuki kitaran Krebs dalam mitokondrion, dan bergabung dengan oksaloasetat untuk membentuk sitrat.[17][18]
- Dua molekul asetil-KoA terkondensasi untuk membentuk asetoasetil-KoA, yang menimbulkan pembentukan asetoasetat dan β-hidroksibutirat.[17] Asetoasetat, β-hidroksibutirat serta hasil penguraian spontannya, aseton,[19] dikenali sebagai badan keton. Badan keton dilepaskan oleh hati ke dalam darah. Semua sel dengan mitokondria boleh mengambil badan keton daripada darah dan menukarkannya semula kepada asetil-KoA, yang kemudiannya boleh digunakan sebagai bahan api dalam kitaran asid sitrik mereka, kerana tiada tisu lain boleh mengalihkan oksaloasetatnya ke dalam laluan glukoneogenesis seperti hati. Tidak seperti asid lemak bebas, badan keton boleh melintasi penghalang darah-otak, dan oleh itu, boleh didapati sebagai bahan api sel sistem saraf pusat, bertindak sebagai pengganti glukosa, di mana sel-sel ini biasanya bertahan.[17] Peningkatan ketara badan keton dalam darah ketika kebuluran, diet rendah karbohidrat, senaman berat berpanjangan dan diabetes melitus 1 yang tidak terkawal, dikenali sebagai ketosis, dan dalam bentuk ekstrem, ketoasidosis.
- Sebaliknya, apabila kepekatan insulin dalam darah tinggi, dan kepekatan glukagon adalah rendah (iaitu selepas makan), asetil-KoA yang dihasilkan oleh glikolisis terpeluwap seperti biasa dengan oksaloasetat, membentuk sitrat dalam mitokondria. Walau bagaimanapun, berbanding meneruskan kitaran asid sitrik lalu ditukar kepada karbon dioksida dan air, sitrat dikeluarkan daripada mitokondria ke dalam sitoplasma.[17] Di sana, ia dibelah oleh liase ATP sitrat menjadi asetil-KoA dan oksaloasetat. Oksaloasetat dikembalikan ke mitokondria sebagai malat (dan kemudian ditukar kembali menjadi oksaloasetat untuk memindahkan lebih banyak asetil-KoA keluar dari mitokondria).[20] Asetil-KoA sitosol ini kemudiannya boleh digunakan untuk mensintesis asid lemak melalui pengkarboksilan oleh asetil-KoA karboksilase menjadi malonil KoA, langkah pertama yang komited dalam sintesis asid lemak.[20][21] Penukaran ini berlaku terutamanya di dalam hati, tisu adipos dan kelenjar susu aktif, di mana asid lemak digabungkan dengan gliserol untuk membentuk trigliserida, takungan bahan api utama kebanyakan haiwan. Asid lemak juga merupakan komponen fosfolipid yang membentuk sebahagian besar dwilapisan lipid daripada semua membran plasma.[17]
- Dalam tumbuhan, sintesis asid lemak de novo berlaku dalam plastid. Banyak biji mengumpul takungan besar minyak biji untuk menyokong percambahan dan pertumbuhan awal anak benih sebelum ia menjadi organisma fotosintesis bersih.
- Asetil-KoA sitosol juga boleh terkondensasi dengan asetoasetil-KoA untuk membentuk 3-hidroksi-3-metilglutaril-CoA (HMG-CoA), langkah pengehad kadar mengawal sintesis kolesterol.[17] Kolesterol boleh digunakan sebagaimana adanya sebagai komponen struktur membran sel, atau ia boleh digunakan untuk mensintesis hormon steroid, garam hempedu dan vitamin D.[17][21]
- Asetil-KoA boleh dikarboksil dalam sitosol oleh asetil-KoA karboksilase, menghasilkan malonil-KoA, substrat yang diperlukan dalam sintesis flavonoid dan poliketida berkaitan, pemanjangan asid lemak untuk menghasilkan lilin, kutikel, dan minyak biji dalam ahli keluarga Brassica, dan pemalonan protein dan fitokimia lain.[22] Dalam tumbuhan, ini termasuk seskuiterpena, brasinosteroid (hormone) dan sterol membran.
- Sintesis steroid:
- Asetil-KoA menyertai laluan mevalonat dengan menyertai sintesis hidroksimetil glutaril-KoA.
- Sintesis asetilkolina:
- Asetil-KoA juga merupakan komponen penting dalam sintesis biogen neurotransmiter asetilkolina. Kolina dalam kombinasi dengan asetil-KoA, dimangkinkan oleh enzim kolina asetiltransferase untuk menghasilkan asetilkolina dan koenzim A sebagai hasil sampingan.
- Sintesis melatonin
- Pengasetilan
- Asetil-KoA juga merupakan sumber kumpulan asetil yang digabungkan ke dalam sisa lisina tertentu protein histon dan bukan histon, dalam pengasetilan pengubahsuaian selepas translasi. Asetilasi ini dimangkinkan oleh asetiltransferase. Asetilasi ini menjejaskan pertumbuhan sel, mitosis dan apoptosis.[23]
- Kawal atur alosterik
- Asetil-KoA berfungsi sebagai pengawal atur alosterik piruvat dehidrogenase kinase (PDK). Ia mengawal selia melalui nisbah asetil-KoA berbanding KoA. Peningkatan kepekatan asetil-KoA mengaktifkan PDK.[24]
- Asetil-KoA merurpakan pengaktif alosterik piruvat karboksilase.[25]
Rujukan
sunting- ^ a b c d Dawson, Rex M. C.; Elliott, Daphne C.; Elliott, William H.; Jones, Kenneth M. (2002). Data for Biochemical Research (ed. 3rd). Clarendon Press. m/s. 117. ISBN 978-0-19-855299-4.
- ^ "Acetyl CoA Crossroads". chemistry.elmhurst.edu. Diarkibkan daripada yang asal pada 2016-11-15. Dicapai pada 2016-11-08.
- ^ "Fatty Acids -- Structure of Acetyl CoA". library.med.utah.edu. Dicapai pada 2017-06-02.
- ^ "All Nobel Prizes in Physiology or Medicine". The Nobel Prize.
- ^ "Metabolic engineering for efficient supply of acetyl-CoA from different carbon sources in Escherichia coli". Microb Cell Fact. 18 (1): 130. August 2019. doi:10.1186/s12934-019-1177-y. PMC 6685171. PMID 31387584.
- ^ "5.12G: The Acetyl-CoA Pathway". 9 May 2017.
- ^ "Central Metabolic Intermediate". MedchemExpress.com. Dicapai pada 15 February 2024.
- ^ Hynes, Michael J.; Murray, Sandra L. (2010-07-01). "ATP-Citrate Lyase Is Required for Production of Cytosolic Acetyl Coenzyme A and Development in Aspergillus nidulans". Eukaryotic Cell (dalam bahasa Inggeris). 9 (7): 1039–1048. doi:10.1128/EC.00080-10. ISSN 1535-9778. PMC 2901662. PMID 20495057.
- ^ Wellen, Kathryn E.; Thompson, Craig B. (2012-04-01). "A two-way street: reciprocal regulation of metabolism and signalling". Nature Reviews Molecular Cell Biology (dalam bahasa Inggeris). 13 (4): 270–276. doi:10.1038/nrm3305. ISSN 1471-0072. PMID 22395772.
- ^ Storey, Kenneth B. (2005-02-25). Functional Metabolism: Regulation and Adaptation (dalam bahasa Inggeris). John Wiley & Sons. ISBN 9780471675570.
- ^ "ACLY ATP citrate lyase [Homo sapiens (human)] - Gene - NCBI". www.ncbi.nlm.nih.gov. Dicapai pada 2016-11-06.
- ^ Ragsdale, S. W. (2004). "Life with carbon monoxide". CRC Critical Reviews in Biochemistry and Molecular Biology. 39 (3): 165–195. doi:10.1080/10409230490496577. PMID 15596550.
- ^ Chatterjea (2004-01-01). Textbook of Biochemistry for Dental/Nursing/Pharmacy Students (dalam bahasa Inggeris). Jaypee Brothers Publishers. ISBN 9788180612046.
- ^ Berg, Jeremy M.; Tymoczko, John L.; Stryer, Lubert (2002). Biochemistry (ed. 5th). W. H. Freeman. ISBN 978-0716730514.
- ^ Blackstock, James C. (2014-06-28). Guide to Biochemistry (dalam bahasa Inggeris). Butterworth-Heinemann. ISBN 9781483183671.
- ^ Houten, Sander Michel; Wanders, Ronald J. A. (2010-03-02). "A general introduction to the biochemistry of mitochondrial fatty acid β-oxidation". Journal of Inherited Metabolic Disease (dalam bahasa Inggeris). 33 (5): 469–477. doi:10.1007/s10545-010-9061-2. ISSN 0141-8955. PMC 2950079. PMID 20195903.
- ^ a b c d e f g Stryer, Lubert (1995). Biochemistry (ed. Fourth). New York: W.H. Freeman and Company. m/s. 510–515, 559–565, 581–613, 614–623, 775–778. ISBN 978-0-7167-2009-6.
- ^ "Oxidation of fatty acids". 2013-10-11.
- ^ "Ketone body metabolism". University of Waterloo.
- ^ a b Ferre, P.; F. Foufelle (2007). "SREBP-1c Transcription Factor and Lipid Homeostasis: Clinical Perspective". Hormone Research. 68 (2): 72–82. doi:10.1159/000100426. PMID 17344645.
this process is outlined graphically in page 73
- ^ a b Voet, Donald; Judith G. Voet; Charlotte W. Pratt (2006). Fundamentals of Biochemistry, 2nd Edition. John Wiley and Sons, Inc. m/s. 547, 556. ISBN 978-0-471-21495-3.
- ^ Fatland, B. L. (2005). "Reverse Genetic Characterization of Cytosolic Acetyl-CoA Generation by ATP-Citrate Lyase in Arabidopsis". The Plant Cell Online. 17 (1): 182–203. doi:10.1105/tpc.104.026211. PMC 544498. PMID 15608338.
- ^ Yi, C. H.; Vakifahmetoglu-Norberg, H.; Yuan, J. (2011-01-01). "Integration of Apoptosis and Metabolism". Cold Spring Harbor Symposia on Quantitative Biology (dalam bahasa Inggeris). 76: 375–387. doi:10.1101/sqb.2011.76.010777. ISSN 0091-7451. PMID 22089928.
- ^ Pettit, Flora H.; Pelley, John W.; Reed, Lester J. (1975-07-22). "Regulation of pyruvate dehydrogenase kinase and phosphatase by acetyl-CoA/CoA and NADH/NAD ratios". Biochemical and Biophysical Research Communications. 65 (2): 575–582. doi:10.1016/S0006-291X(75)80185-9. PMID 167775.
- ^ Jitrapakdee, Sarawut; Maurice, Martin St.; Rayment, Ivan; Cleland, W. Wallace; Wallace, John C.; Attwood, Paul V. (2008-08-01). "Structure, Mechanism and Regulation of Pyruvate Carboxylase". The Biochemical Journal. 413 (3): 369–387. doi:10.1042/BJ20080709. ISSN 0264-6021. PMC 2859305. PMID 18613815.
Pautan luar
sunting- Acetyl+Coenzyme+A dalam Tajuk Subjek Perubatan (MeSH) di Perpustakaan Perubatan Negara AS